Влияние прогестерона на заболевания предстательной железы и перспективы его использования для профилактики и лечения доброкачественной гиперплазии предстательной железы
Наиболее распространенными патологиями предстательной железы у мужчин после 40 лет являются доброкачественная гиперплазия предстательной железы (ДГПЖ) и рак предстательной железы (РПЖ).
Эпидемиология и роль некоторых гормонов
Действительно, если в среднем возрасте около 40 лет распространенность ДГПЖ не выходит за 10%, то после 70 лет она встречается у подавляющего большинства мужчин, не менее чем в 80% случаев. Кроме того, ДГПЖ прогрессивно увеличивается в своей распространенности, она стремительно повышает риски малигнизации предстательной железы, а РПЖ является наиболее часто встречающимся раком в мужской популяции и второй причиной смерти от злокачественных неоплазий.
Важно отметить еще один существенный аспект в повышении риска развития РПЖ кроме возраста – этническая принадлежность. Достаточно много работ, демонстрирующих большую предрасположенность к РПЖ темнокожих представителей мужской популяции в сравнении с белыми мужчинами, в том числе называется одна из возможных причин – более высокий уровень эстрадиола у представителей негроидной расы и латиноамериканцев. Хотя достаточно долго основным этническим различием считалась разница в уровне тестостерона и предполагалось, что он существенно выше у представителей негроидной расы или южных стран. И, несмотря на то, что заболевания предстательной железы прогрессивно увеличиваются во всем мире, прорывных открытий в лечении или профилактике пока нет, как нет и новых данных о патогенезе и роли разных гормонов в механизме развития ДГПЖ или РПЖ, в том числе, о роли прогестерона.
ДГПЖ – это увеличение объема простаты, в основе которого лежит, преимущественно, клеточная пролиферация переходной зоны.
РПЖ – это злокачественное перерождение эпителиальных клеток ткани предстательной железы.
По данным ФГБУ «НМИЦ радиологии» МЗ РФ за 15 лет с 2001 года рост РПЖ в РФ увеличился в 5 раз с 10,01 до 57,22 случаев на 100 тысяч населения. С 2016 года в нашей стране отмечено новых 38371 случаев РПЖ, а среднегодовой темп прироста заболеваемости РПЖ составил 7,12% случаев.
Рассматривать патогенез развития ДГПЖ и РПЖ в аспекте всех гормонов не является целью. Но то, что гормоны играют ключевую роль в развитии этих заболеваний, нет сомнений и обозначить широкими мазками то, как действуют разные гормоны в предстательной железе, важно, так как это может помочь осветить действие того гормона, который незаслуженно долго остается в тени, а именно прогестерона.
Андрогены
Андрогены действуют в эпителиальной и стромальной тканях предстательной железы через андрогеновый рецептор, один рецептор на два гормона: тестостерон и дигидротестостерон. Во время полового созревания примерно к 20 годам под действием андрогенов предстательная железа увеличивается с 10 до 20 грамм, а в среднем возрасте начинается пролиферация переходной зоны, окружающей уретру, при том, что уровень андрогенов начинает снижаться .
Гормоны щитовидной железы
Участвуют в клеточном росте, метаболизме и дифференцировке, в том числе и тканей предстательной железы.
Эпидемиологические исследования показали, что мужчины с ДГПЖ или РПЖ имеют значительно повышенный уровень трийодтиронина (Т3) и тироксина (Т4) и сниженные уровня тиреотропного гормона (ТТГ) у пациентов с ДГПЖ по сравнению с контрольной группой. Также свободный Т3 положительно, а ТТГ отрицательно коррелирует с объемом простаты.
Пациенты с гипотиреозом имеют меньший риск развития РПЖ по сравнению с эутиреоидными мужчинами, что было подтверждено данными метаанализа 2020 года. В ряде исследований было продемонстрировано, что Т3 увеличивает пролиферацию клеток РПЖ in vitro/in vivo и экспрессию ПСА. Экспериментальные исследования также показали, что тиреоидные гормоны способствуют канцерогенезу, индуцируя ангиогенез. Много ли специалистов эндокринологов, тем более урологов, связывают ДГПЖ с нарушением баланса гормонов щитовидной железы?
Инсулиноподобный фактор роста 1 (ИФР-1) и гормон роста (ГР)
Большое количество исследований показывает, что эндокринная ось ГР-ИФР-1 играет ключевую роль в росте и развитии простаты в нормальной физиологии, а также в патологических состояниях. ИФР-1 секретируется в основном печенью при стимуляции ГР, но он также экспрессируется локально в стромальных и эпителиальных клетках простаты, где он может действовать аутокринным/паракринным образом. Связывание ИФР-1 с рецептором ИФР-1 или рецептором инсулина в предстательной железе активирует путь фосфоинозитид 3-киназы (PI3K)/протеинкиназы B (АКТ) и путь RAF/MAPK, которые способствуют выживанию и пролиферации клеток.
В ряде исследований показана большая распространенность ДГПЖ у пациентов с акромегалией. Они обнаружили, что у пациентов с акромегалией наблюдается более высокий IPSS (International Prostate Symptom Score – международная система суммарной оценки заболеваний предстательной железы), повышенная скорость увеличения простаты при ректальном исследовании и УЗИ, более высокие уровни ПСА и обструктивный паттерн при урофлоуметрии, а также структурные изменения простаты, независимо от их возраста, активности заболевания или гонадного статуса. Эти результаты свидетельствуют о том, что гиперактивация оси ГР/ИФР-1 играет важную роль в патогенезе ДГПЖ у пациентов с акромегалией. Это дополнительно подтверждается уменьшением объема простаты у пациентов с неактивным заболеванием (более 24 месяцев).
Эпидемиологические исследования показали, что высокие уровни циркулирующего ИФР-1 связаны с повышенным риском рака простаты, особенно запущенного заболевания. Более того, экспрессия компонентов осей гормона роста, инсулина и ИФР-1 может тонко модулироваться в простате такими факторами окружающей среды, как диета. Как было описано ранее, ожирение способствует структурным изменениям в простате.
Недавние исследования выявили участие не только сигнализации ИФР-1, но и самого ГР, который участвует в развитии нескольких опухолей, включая рак простаты. Было показано, что антагонисты соматотропин-рилизинг-гормона напрямую уменьшают объем простаты, не задействуя андрогенный путь. Примечательно, что ИФР-1 обычно снижается с возрастом, хотя метаболические нарушения и акромегалия приводят к увеличению этого гормона, поэтому уровни ИФР-1 следует оценивать у пациентов с заболеваниями простаты, с сопутствующим сахарным диабетом или другими метаболическими изменениями, а также с акромегалией.
Известно, что гиперинсулинемия усиливает пролиферацию эпителиальных клеток простаты in vitro и, наоборот, гипоинсулинемия уменьшает объем простаты. В соответствии с этими результатами, пациенты с уровнем инсулина в сыворотке >13 мЕд/л имеют больший объем простаты и ежегодную скорость роста ДГПЖ по сравнению с пациентами с уровнем инсулина <7 мЕд/л.
Инсулинорезистентность является независимым предиктором развития СНМП (синдрома нижних мочевых путей). Это может быть связано с гиперактивностью автономной нервной системы, в основном с участием α-адренергического пути, который тесно связан с гиперинсулинемией и участвует в патогенезе СНМП. Повышенный ИМТ >35 кг/м2 был связан с 3,5-кратным повышением риска развития ДГПЖ (>40 мл) и с 1,2-кратным повышением риска развития СНМП по сравнению с теми, у кого ИМТ <25 кг/м2. Данные, полученные у 21694 пациентов, подтвердили эти выводы, показав, что ИМТ является предиктором развития СНМП.
Ряд авторов предложили рассматривать РПЖ как компонент МС (метаболического синдрома), поскольку гиперинсулинемия проспективно является фактором риска смерти от РПЖ. Долгосрочный анализ выживаемости, проведенный на 2546 пациентах, у которых развился рак предстательной железы, показал: у людей с избыточным весом и высоким уровнем С-пептида риск смертности в четыре раза выше, чем у пациентов с ИМТ <25 кг/м2 и низким уровнем С-пептида, независимо от других клинических предикторов.
Эстрогены
Рецепторы эстрогенов, как ERα, так и ERβ, представлены в простате, что говорит об активности эстрогенов в этом органе. Место расположения определяет их эффекты. Например, ERα, которые связывают в большей степени с провоспалительными эффектами, в основном находятся в стромальных клетках, и их экспрессия стимулирует рост, как стромальных, так и эпителиальных клеток простаты, в том числе путем воздействия паракринных медиаторов, таких как стромальный bFGF, эпидермальный фактор роста (EGF) и ИФР-1. И именно с активацией этих рецепторов связывают гиперплазию простаты, воспаление и высокий показатель Глисона, а также плохую выживаемость пациентов с РПЖ.
Эпидемиологические исследования подтвердили роль эстрогенов в РПЖ. Афроамериканские мужчины, у которых были выявлены более высокие уровни эстрадиола в сыворотке, представляют повышенный риск развития РПЖ, в сравнении с представителями белой расы. А ERβ, обладающие противовоспалительными свойствами, находятся в эпителиальных клетках, иначе говоря, на рост стромальной ткани они не влияют.
Доклинические и клинические результаты демонстрируют, что агонисты ERβ могут быть эффективны в терапии РПЖ, особенно на ранней стадии. Иначе говоря, эстрогены и ERα, могут рассматриваться, как терапевтическая цель при ДГПЖ. Можно воздействовать на ароматазу, предотвращая конвертацию тестостерона в эстрадиол. Или использовать селективные модуляторы эстрогеновых рецепторов (SERM), которые продемонстрировали антипролиферативное действие на ткань простаты. Также важно отметить, что возрастные изменения половых гормонов, в частности, дефицит тестостерона и повышение уровня эстрогенов, на фоне ожирения, играют ключевую роль в патогенезе возрастных заболеваний предстательной железы.
Лептин
Лептин, гормон, вырабатываемый адипоцитами, стимулирует рост клеток простаты. Этот эффект может быть связан с тем, что лептин индуцирует экспрессию ароматазы, соответственно, повышая уровень эстрогенов в крови, а их действие в избытке на простату описано выше.
Тестостерон
Приводятся убедительные данные не только безопасного, но и эффективного использования тестостеронзаместительной терапии (ТЗТ) у пациентов с дефицитом андрогенов, метаболическими нарушениями и ДГПЖ, существенно улучшающую качество жизни пациентов, в том числе после операции при РПЖ при соблюдении ряда условий.
И конечно же, в ткани предстательной железы представлены рецепторы не только перечисленных выше гормонов, но и других. Например, прогестерона, влиянию которого на предстательную железу пока уделено значительно меньше внимания, чем другим гормонам.
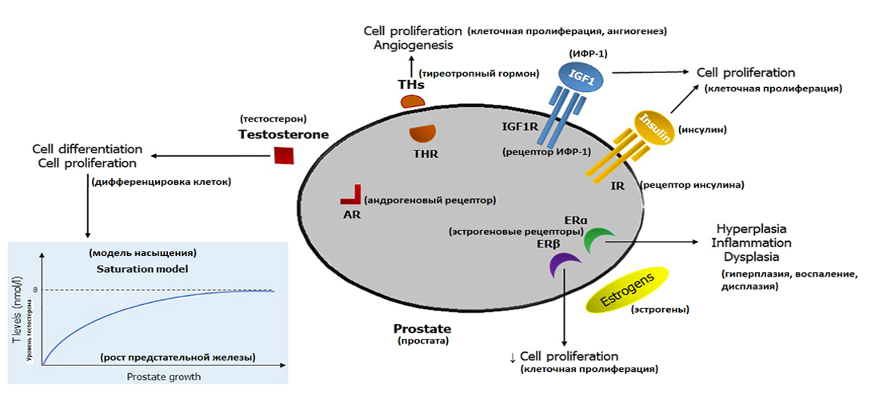
Несмотря на то, что схема стероидогенеза не имеет половых различий, у многих клиницистов гормон прогестерон стойко ассоциируется с функционированием женской половой системы, причем, только в репродуктивном аспекте.
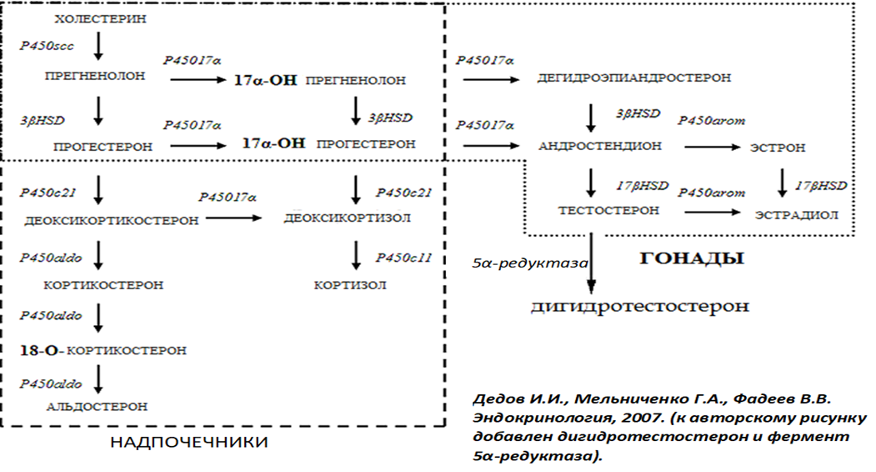
Но, для мужского организма прогестерон также важен, как и для женского, причем, на протяжении всей жизни. Его механизмы действия и эффекты, в том числе и в аспекте ДГПЖ мы рассмотрим подробнее в следующих частях.
Прогестерон – стероидный гормон, вырабатываемый в организме у мужчин в небольшом количестве в тканях яичек и в надпочечниках из холестерина. Кроме того — в других органах, включая ЦНС. Химическая формула – С21Н30О2. В сутки в мужском организме вырабатывается от 1,5 до 3 мг гормона, а после 60 лет прогрессивно снижается и составляет 0,38-0,13 нг/мл. Именно со снижением уровня прогестерона в крови и снижением протективного иммунологического эффекта связывают более тяжелое течение аутоиммунных и инфекционных заболеваний у лиц старшего возраста. Прогестерон является предшественником половых, нейростероидных, минералкортикоидных гормонов и прежде всего кортизола, как видно из схемы стероидогенеза.
Натуральный прогестерон:
1. поддерживает низкий уровень сывороточного эстрадиола, увеличивая скорость конверсии эстрадиола в менее активный эстрон (в свете постоянно растущего количества мужчин с ожирением, соответственно, с развитием воспаления жировой ткани и гиперэстрогенией, это свойство приобретает особое значение);
2. оказывает кардиопротективный эффект;
3. способствует синтезу ФСГ (фолликулостимулирующий гормон), повышает качество сперматогенеза (вопрос о безопасности использования прогестерона в репродуктивных технологиях можно экстраполировать через широкое использование прогестерона у беременных и при проведении ВРТ (вспомогательные репродуктивные технологии) у женщин, что демонстрирует отсутствие токсичности прогестерона и прогестинов как в общей, так и репродуктивной сферах медицины);
4. в малых дозах стимулирует, а в больших подавляет синтез ЛГ (лютеинизирующий гормон);
5. способствует снижению повышенного уровня дигидротестостерона, за счет снижения активности 5-αредуктазы, что принципиально важно в аспекте развития ДГПЖ и РПЖ;
6. влияет на центральную и периферическую нервную системы, обладая нейропротективной способностью и оказывая седативный эффект.
Метаболит прогестерона – 5-альфа-прегнанолон – обладает антидисфорической активностью, участвует в регулировании процессов сна и бодрствования и, возможно, оказывает нейропротекторный эффект после повреждения мозговой ткани.
Стимулирующее дыхательный центр действие прогестерона и повышающее его чувствительность к уровням СО2 и О2, достаточно долгое время поддерживало надежду у ученых на использование прогестерона в качестве лечебного средства у пациентов с обструктивным апноэ сна.
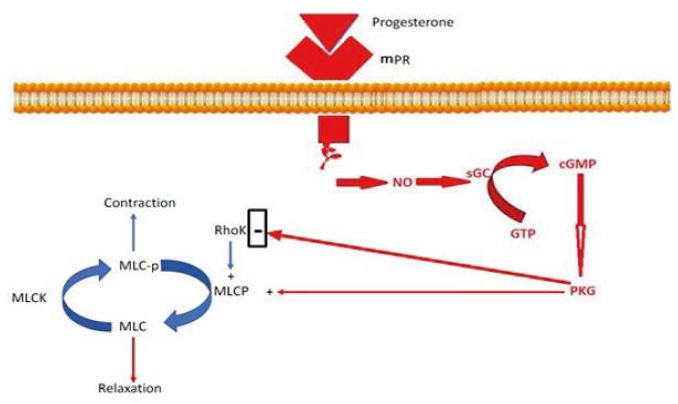
Или, известно, что прогестерон оказывает ингибирующее действие на гладкомышечные клетки сосудистой стенки и не только кишечника, например, отчасти за счет повышения синтеза оксида азота. Он вызывает образование циклического гуанозинмонофосфата (цГМФ), который активирует протеинкиназу G (PKG), которая играет ключевую роль при релаксации гладкой мускулатуры.
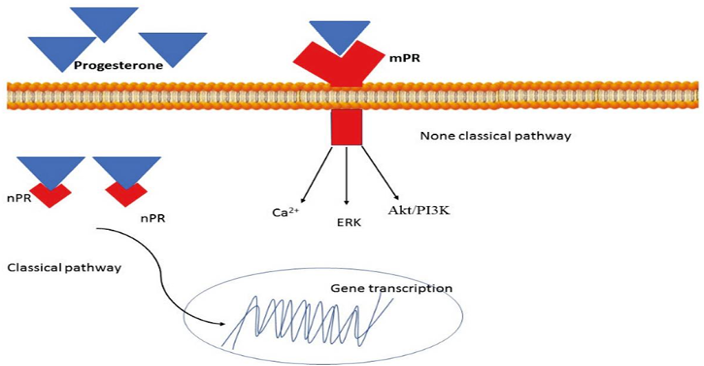
Производство NO приводит к образованию цГМФ и к активации PКG. PКG ингибирует сигнальные пути, стимулирующие сокращение, такие, как RhoK, и активирует передачу сигналов, которая приводит к расслаблению мышц, например MLCP. mPR: рецептор прогестерона, NO: оксид азота, цГМФ: циклический гуанозинмонофосфат, GTP: гуанозинтрифосфат, PKG: протеинкиназа G, RhoK: Rho киназа, MLCP: фосфатаза легкой цепи миозина.
Воздействие на индукцию синтеза азота мы можем проецировать на всю сердечно-сосудистую систему и здесь также сложно провести разделение по половому признаку или переоценить важность этого свойства, как у мужчин (тот же сосудистый механизм эрекции основан на действии оксида азота), так и у женщин.
При этом, возникает понимание постменопаузального повышения риска развития сердечно-сосудистых заболеваний у женщин, которое всегда связывалось исключительно со снижением уровня эстрогенов и, к сожалению, прогестерон оставался в тени. Хотя его синтез даже ранее, чем уровень эстрогенов, заметно снижается еще до наступления менопаузы.
Но, есть еще интересные данные, где оценивались изменения углеводного обмена у женщин в связи с изменением уровня прогестерона. Было выяснено, что он ингибирует поглощение глюкозы и увеличивает глюконеогенез печенью, то есть формируется картина, характерная для инсулинорезистентности. И здесь важно сделать акцент на том, что уже давно приковывает внимание многих ученых – это взаимосвязь роста числа случаев развития ДГПЖ и РПЖ у мужчин с ожирением и метаболическим синдромом. Кроме того, в центральной нервной системе (ЦНС) прогестерон, наоборот, улучшал показатели углеводного обмена за счет увеличения синтеза транспортных белков глюкозы. С этим, в том числе, связывают нейропротекторный эффект прогестерона в отношении ЦНС. А также, взаимодействие с рецепторным комплексом ГАМК A в ЦНС, включая седативное и анестезирующее действие.
Нельзя упустить еще один важный аспект действия прогестерона – иммунологический: прогестерон модулирует процесс дифференцировки Т-лимфоцитов в направлении Th2, контролирует цитотоксичность клеток – естественных киллеров (natural killer cell, NK-клетки) и синтез провоспалительных цитокинов (интерлейкины (ИЛ) – ИЛ-4, ИЛ-6 и др.). Несмотря на то, что интерес к прогестерону у мужчин эпизодически проявлялся в разных научных школах, он не имел широкого резонанса. Последним пиком этого интереса был период пандемии коронавирусной инфекции, когда в период лечения мужчин с КОВИД-19 были продемонстрированы противовоспалительные и иммуномодулирующие эффекты прогестерона, период лечения был короче и потребность в кислороде сокращалась на 3 дня. Также было отмечено, что у пациентов с атипичной пневмонией уровень прогестерона в крови был снижен. В другом исследовании было показано, что прогестерон снижает синтез IL-1β, IL-6, TNFα, IL-12, хемокинов (белка-1 MCP-1/CCL2).
Отдельно важно сделать акцент на том, что прогестерон оказывает на эндотелий сосудов защитное действие, которое реализуется только при физиологических уровнях прогестерона и его гомологичной структуре, соответствующей натуральному прогестерону. Усиленная стимуляция рецепторов эндотелия в процессе лечения синтетическими прогестинами приводит к изменению его функции путем влияния на вазодилатацию, транспорт липидов, адгезию белков и, как следствие, к изменению морфологического состояния сосудистой стенки.
Следует отметить, что синтетические гестагены хорошо переносятся пациентами, но их прием противопоказан во время беременности, у пациенток с нарушением функции печени, у больных с раком молочной железы, заболеваниями сосудов головного мозга и дисфункцией коронарных артерий, у женщин с отягощенным анамнезом по возникновению тромбоэмболии, а также у курящих пациенток. Все синтетические прогестины создавались по принципу их высокой аффинности и длительности взаимодействия с прогестероновыми рецепторами. В результате оказалось, что слишком сильная связь синтетических прогестинов с рецепторами эндотелия увеличивает риск развития сердечно-сосудистых заболеваний у приматов и людей. Несмотря на то, что представленные данные относятся к женской части популяции, мы можем экстраполировать эти результаты и на мужчин, но для подтверждения данных тезисов необходимо проведение исследований.
Действие прогестерона определяется за счет активации классических и неклассических сигнальных путей. Приоритетным является классический путь, когда прогестерон связывается со своим рецептором из суперсемейства ядерных рецепторов факторов транскрипции. Существуют две основные изоформы рецепторов прогестерона (PR): PR-A и PR-B. Соединение молекулы прогестерона с его рецептором в гормонрецепторный комплекс индуцирует его транслокацию в ядро, где инициируется транскрипция широкого спектра белков (образование информационной РНК, которая транслируется рибосомами для производства специфических белков). Существует и неклассический путь, который производит более быстрые действия путем активации рецепторов на клеточной мембране, которые напоминают рецепторы, связанные с G-белком. Связывание прогестина с этими рецепторами быстро активирует различные внутриклеточные сигнальные молекулы, такие как, например, повышение уровня внутриклеточного кальция (с этим же связывают воздействие прогестерона на сперматогенез.)
Прогестерон имеет родственную связь не только с прогестероновыми рецепторами, но также и с рецепторами эстрадиола, кортизола, тестостерона и альдостерона. Прогестерон способен конкурировать с альдостероном за рецепторы, расположенные в почках и в большей степени в стенках артерий.
Очевидно, одним из наиболее интересных фактов является факт действия прогестерона в гладкомышечных клетках сосудистой стенки, которое приводит к гипотензивному действию на организм человека и ингибирует ангиотензин II-индуцированное сокращение гладкомышечных клеток в сосудистой стенке.
Прогестерон может оказывать релаксирующий эффект на гладкомышечные клетки несколькими путями, кроме воздействия на мембранные белки, с активацией ингибирующего G-белка, внутриклеточных сигнальных путей с повышением внутриклеточного уровня оксида азота, с последующим угнетением сокращения гладкой мускулатуры. Другой путь это – активация циклического аденозинмонофосфата (цАМФ), который подавляет сократительную активность за счет уменьшения легкой цепи миозина-20 (MLC-20). И в этом контексте снова стоит упомянуть об эректильной функции и возможной недостающей цепи в патогенезе эректильной дисфункции – недостаток прогестерона или нарушенный баланс стероидных гормонов в отношении прогестерона.
Здесь вполне уместно задаться вопросом, а есть ли какие-то интересные результаты исследований с использованием прогестерона в мировой литературе? Достаточно много ученых и врачей-андрологов возлагают надежды на использование прогестерона в борьбе с мужским бесплодием. В исследовании, проведенном в 2022 г., в 20 образцов спермы с астенозооспермией добавляли синтезированные твердые наночастицы прогестерона и оценивали их влияние на ряд показателей.
Были получены следующие результаты:
1. Прогестерон повышал целостность мембран сперматозоидов (p < 0,05).
2. Прогестерон усиливал акросомальную реакцию и в целом капацитацию (способность проникать в яйцеклетку) (p < 0,05).
3. Повышался уровень общей антиоксидантной способности (p < 0,05).
4. Усиливалась экспрессия генов PTK, PKA, SPACA1 и P38MAPK (p < 0,001).
Иначе говоря, оказывалось очевидное положительное влияние на показатели сперматогенеза, что повышает заинтересованность ученых в проведении дальнейших исследований в аспекте использования препаратов прогестерона для улучшения сперматогенеза у мужчин с бесплодием.
Дигидротестостерон
Так как одна из ведущих ролей в патогенезе ДГПЖ принадлежит дигидротестостерону, то и поиски эффективных средств, способных привести к балансу этого гормона, являются приоритетными. Результаты одного из экспериментальных исследований, проведенного уже более 30 лет назад, не теряют своей ценности и помогают оценить эффективность прогестерона и других гормонов и лекарственных средств в отношении изменения активности фермента 5 α-редуктазы и, соответственно, уровня дигидротестостерона. Протокол исследования предполагал смешивание клеток нормальной кожи половых органов и лобка с физиологическими концентрациями тестостерона для оценки активности 5 α-редуктазы по ее превращению в дигидротестостерон, используя уровень дигидротестостерона как индикатор степени ингибирования 5 α-редуктазы. В отдельных экспериментах активность 5 α-редуктазы оценивали до и после добавления натурального прогестерона, медроксипрогестерона ацетата, левоноргестрела, норэтиндрона, 17-бета-эстрадиола и этинилэстрадиола. Каковы же результаты: эффективность натурального прогестерона в ингибировании активности 5 α-редуктазы неоспоримо выше других гормонов, которые связывали с подавлением активности фермента 5 α-редуктазы.
Если обратить внимание на наиболее широко используемый класс препаратов у пациентов с ДГПЖ, уменьшающих объем предстательной железы и останавливающих рост ее тканей через ингибирование тестостерон-5-альфа-редуктазы, то в своей химической основе эти препараты практически идентичны молекуле прогестерона.
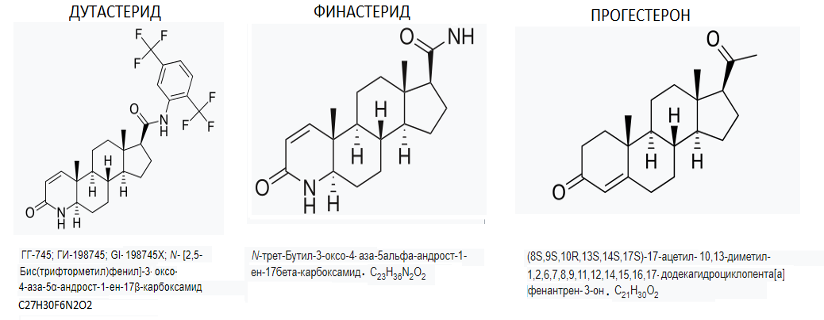
Почему же мало исследований, посвященных использованию прогестерона в лечении ДГПЖ или РПЖ? Они демонстрируют негативное влияние на эти заболевания.
Например, в одном из исследований, посвященных раку предстательной железы, прогестерон рассматривается, как один из онкомаркеров и онкометаболитов, и его депривация потенциально может улучшить прогнозы лечения. Накапливающиеся данные также демонстрируют, что происходит мутация рецепторов в клетках предстательной железы при раке. И эти клетки могут реагировать и активироваться, в том числе и кортикостероидами, кроме андрогенов или прогестерона.
При этом сложно отрицать провоспалительную основу любого онкопроцесса. А из данных физиологии и множества исследований, прогестерон демонстрирует способность снижать синтез провоспалительных цитокинов, например, IL-1β и фактора некроза опухоли-альфа, в том числе и при воспалительных заболеваниях ЖКТ, что можно экстраполировать на другие органы и системы. Отмечено повышение экспрессии классических рецепторов прогестерона в простате при ДГПЖ, а также раке простаты, что может быть следствием патологических процессов или одним из их триггеров. Пока это остается вопросом. Также отмечено повышение количества андрогеновых рецепторов в целом и их накопление в ядре под воздействием прогестерона.
Очень важно понимать, что одни и те же гормоны в физиологических и патологических условиях могут оказывать противоположный эффект, и подавлять синтез этих гормонов –прогестерона и андрогенов – в качестве профилактики онкопроцессов, ошибочно. В то же время при уже сформированном онкопроцессе подходы к использованию любых гормонов в лечении меняются. Чаще всего их использование противопоказано.
Таким образом, складывается понимание о системности действия прогестерона в организме как женщин, так и мужчин, и это вполне характерно для действия гормонов в целом. Важно понять, каково же действие прогестерона относительно предстательной железы и может ли нормализация баланса не только андрогенов, эстрогенов, но и прогестерона, способствовать профилактики развития ДГПЖ и РПЖ или использоваться в качестве лечебного средства. Может возникнуть логичный вопрос – зачем нужно исследовать эффективность прогестерона, если широко используемые препараты Финастерид или Дутастерид достаточно эффективны? Финастерид снижает ДГТ в сыворотке или простате на 71 % или 85% соответственно, в то время как дутастерид снижает ДГТ, как в сыворотке, так и в простате на 95% и более. Это очень высокая эффективность! Но андрогеновый рецептор (АР) может функционировать по-разному, когда соотношение тестостерона и ДГТ нарушается из-за гомеостаза, и эти различия могут усиливаться при лечении различными препаратами. Финастерид и Дутастерид могут иметь нецелевые эффекты, которые напрямую ингибируют АР. Дутастерид снижает уровень внутриклеточного тестостерона практически до неопределяемого уровня. Финастерид одинаково хорошо блокировал накопление тестостерона в каждой клеточной линии. Доза 0,5 мкМ Финастерида устраняла любые следы тестостерона внутри клеток. Результаты применения Дутастерида и Финастерида позволяют предположить, что эти ингибиторы 5 α-редуктазы также могут блокировать поглощение тестостерона клетками. Именно поэтому, возможно, мы часто фиксируем те самые побочные эффекты: снижение либидо, эректильную дисфункцию, преждевременную эякуляцию и гинекомастию, когда назначаем эти препараты.
Проведение исследования с использованием натуральных форм прогестерона может обеспечить снижение уровня дигидротестостерона, относительно или абсолютно увеличенного, и уменьшение объема предстательной железы. А также улучшение эректильной функции, нормализацию либидо и других важных функций мужского организма.


