Лечение острых лейкозов без химиотерапии
Острые лейкозы – группа жизнеугрожающих злокачественных заболеваний системы крови, субстратом которых являются клетки костного мозга, трансформировавшиеся в опухолевые. Это определение объединяет множество заболеваний, различных по клиническим проявлениям, биологическим особенностям, терапевтическому подходу.
Успехи гематологии, достигнутые в последние десятилетия, позволили полностью излечивать или же достигать длительных стойких ремиссий при многих ранее неизлечимых заболеваниях системы крови. Одними из наиболее значимых и ярких прорывов в терапии острых лейкозов являются успехи в лечении острого промиелоцитарного лейкоза (ОПЛ), варианта острого лейкоза, характеризующегося в дебюте в большинстве случаев крайне агрессивным течением с высокой вероятностью гибели пациента, однако благодаря современным подходам к противоопухолевой и сопроводительной терапии в настоящее время ставшего наиболее прогностически благоприятным.
Изменение подходов к терапии ОПЛ хорошо демонстрирует эволюцию методов лечения, применяемых в онкологии: менее эффективные методы терапии замещаются действенными, более токсичные – более безопасными.
ОПЛ – очень редкое заболевание. Так, частота заболеваемости ОПЛ, по данным Европейского ракового регистра HAEMACARE, составляет 0,14 случая на 100 000 населения в год. Точных данных по заболеваемости ОПЛ в России нет, но, по данным Российского выборочного регистрационного исследования, выполненного в ФГБУ «НМИЦ гематологии» Минздрава России с 2013 по 2016 год с включением 334 пациентов из 5 российских региональных гематологических центров и отделений, ОПЛ диагностировали в 5% случаев всех острых лейкозов. Заболевание встречается у пациентов всех возрастных групп, но чаще всего у взрослых до 60 лет.
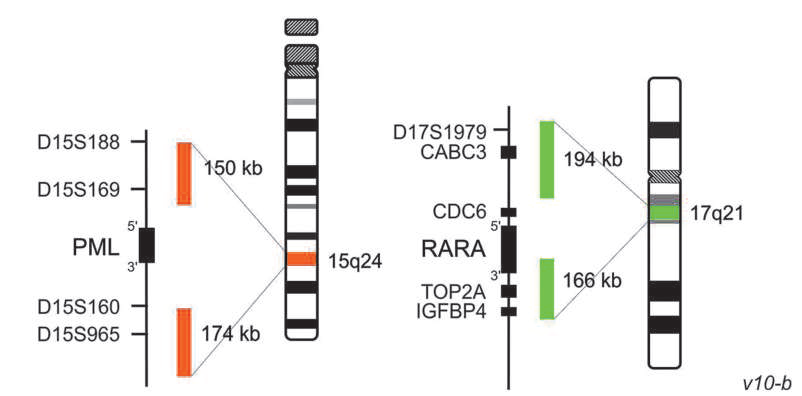
возникновении транслокации t(15;17)
Для опухолевых клеток ОПЛ обязательно наличие определенной генетической перестройки – транслокации между хромосомами 15 и 17 – t(15;17), которая приводит к образованию аномального гена PML::RARA. Накопление кодируемого им белка и отсутствие нормальных продуктов генов PML и RARA приводят к пролиферации опухолевых клеток и прекращению их дифференцировки на этапе промиелоцитов – возникает «блок дифференцировки» – клетка приобретает новый фенотип или начинает дифференцировку предшественников клеток, которые отличаются от родительской.
Накопление большой опухолевой массы в костном мозге подавляет выработку нормальных клеток крови: лейкоцитов, тромбоцитов и эритроцитов. Это приводит к возникновению инфекционных осложнений, развитию кровотечений и анемии соответственно. Кроме того, опухолевые промиелоциты, по сравнению с опухолевыми клетками при других вариантах острых лейкозов, в большом количестве содержат молекулы, способствующие разрушению соединений, ответственных за свертывание крови, в первую очередь фибриногена. Это значительно усугубляет проявления геморрагического синдрома, который при ОПЛ является ведущим проявлением заболевания и может принимать всевозможные формы: от множественных синяков и петехий до кровоизлияний в головной мозг. Именно фатальные кровотечения, особенно при задержке начала противоопухолевого лечения, чаще всего приводят к смерти пациентов. Таким образом, для пациентов с ОПЛ крайне важно быстро и точно установить диагноз.
Диагностика
При выполнении анализа крови врачи из-за подавления опухолью нормальной работы костного мозга чаще всего сталкиваются со снижением содержания всех форменных элементов: лейкоцитов, эритроцитов, тромбоцитов. Но примерно в четверти случаев количество лейкоцитов может превышать нормальные значения за счет опухолевых промиелоцитов. Как правило, в таких случаях проявления кровоточивости более выраженные, а лечение может привести к большей частоте осложнений. Поэтому количество лейкоцитов имеет важное значение при диагностике ОПЛ.
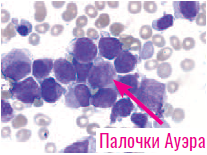
В зависимости от исходного числа лейкоцитов в анализе крови пациентов распределяют на группы низкого и высокого риска, что обязательно учитывается при проведении противоопухолевого и сопроводительного лечения.
Обнаружение подобных клеток в крови и костном мозге, особенно вкупе с выраженной кровоточивостью и со снижением концентрации фибриногена, должно незамедлительно направить диагностический поиск в сторону ОПЛ. Но только обнаружение t(15;17) и/или гена PML::RARA в клетках костного мозга по результатам цитогенетического исследования (кариотипирование или FISH-исследование) или полимеразной цепной реакции является подтверждением этого диагноза.
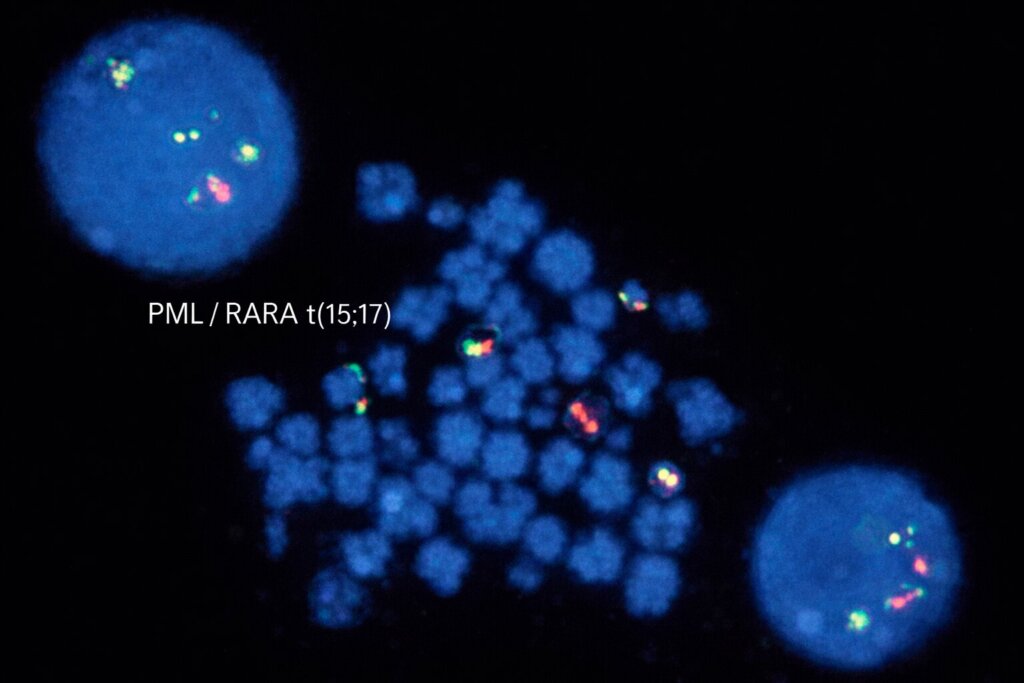
Обнаружение t(15;17) при помощи
FISH-исследования. Зонды к PML и RARA связываются с участками 15 и 17 хромосом соответственно. При отсутствии транслокации в клетке выявляются по два отдельных красных и зеленых сигнала, а при наличии t(15;17) они сливаются и выявляется красно-зеленый или желтый сигнал.
Терапия: история
ОПЛ, часто протекающий так драматично из-за серьезных кровотечений и низкой эффективности химиотерапии, до 80-х годов прошлого века был «плохой новостью» для врачей. Однако в 1985 году внедрение шанхайскими исследователями в практику терапии полностью транс-ретиноевой кислотой (All-trans Retinoic Acid, ATRA) производного витамина А – совершило революцию в лечении этого заболевания.
Химиопрепараты, или цитостатические препараты, непосредственно или опосредованно приводят к разрушению опухолевых клеток. Чувствительность к такой терапии не в последнюю очередь связана со способностью опухоли активно делиться (химиотерапия, как правило, эффективна против быстро делящихся клеток, таких как раковые). Этой же способностью обладают и некоторые нормальные клетки организма человека: клетки кожи и слизистых оболочек, нормальные стволовые клетки костного мозга, клетки печени, что приводит к неизбежным осложнениям химиотерапии даже у пациентов, находящихся в ремиссии (ведь продолжение лечения для закрепления эффекта в течение определенного времени необходимо и после достижения ремиссии!). Не следует также забывать о том, что влияние цитостатических препаратов на нормальные стволовые клетки, пусть и редко, но может привести к развитию других опухолевых заболеваний.
Механизм действия ATRA
ATRA, в отличие от цитостатических препаратов, за счет подавления работы аномального гена PML::RARA и его продуктов устраняет «блок дифференцировки»: опухолевые промиелоциты, проходя все этапы дифференцировки, постепенно превращаются в зрелые гранулоциты и закономерно погибают. Кроме того, ATRA действует целенаправленно на клетки – носители гена PML::RARA.
Даже без использования химиотерапии применение ATRA позволяет успешно достигать ремиссий, правда, непродолжительных. А добавление к ATRA химиотерапии позволило достичь в 1990-х годах головокружительных для гематологии того времени результатов: устойчивой ремиссии в 90–95% случаев и 6-летней безрецидивной выживаемости до 86%. Кроме того, проявления столь опасного при ОПЛ геморрагического синдрома уже после нескольких дней лечения ATRA сходят на нет.
Однако химиотерапия даже в сочетании с ATRA в силу механизма своего действия неизбежно связана с токсическими осложнениями: повреждением слизистых и кожи и нарушением их барьерной функции, нарушением работы печени, посткурсовым снижением концентраций гемоглобина, тромбоцитов и лейкоцитов, вторичным иммунодефицитом. При этом достижение ремиссии и отсутствие проявлений опухолевого заболевания не гарантирует, что осложнений химиотерапии не будет. Они приводят к дополнительным проблемам со здоровьем, необходимости применения порой дорогостоящих и токсичных лекарственных препаратов, потере для пациента связи с обществом за счет длительного пребывания в больнице. Именно поэтому, несмотря на высокую эффективность терапии, на протяжении следующих десятилетий исследователи неустанно работали над совершенствованием протоколов лечения и сопроводительной терапии, направленных на уменьшение летальных исходов, вероятности развития рецидивов, минимизацию токсичности и улучшение качества жизни пациентов.
Прорыв в лечении ОПЛ
В 1992 году китайский исследователь H. Sun с коллегами опубликовали работу, которая наглядно показала, что триоксид мышьяка (АТО – от англ. arsenic trioxide) в низких дозах, вводимый внутривенно, является эффективным препаратом для лечения ОПЛ. Как и ATRA, это «таргетный» препарат, который действует, устраняя «блок дифференцировки» опухолевых промиелоцитов. Дальнейшие исследования подтвердили противоопухолевую активность ATO и продемонстрировали, что его сочетание с ATRA способствует дальнейшему улучшению результатов лечения ОПЛ, позволяя достичь более высоких показателей выживаемости пациентов, а также значимого уменьшения токсичности проводимой терапии.
Кроме того, терапия после достижения ремиссии не приводит к развитию осложнений, которые бы потребовали госпитализации пациента в круглосуточный стационар, и большая часть лечения проходит в амбулаторных условиях. В настоящее время применение схем терапии ОПЛ с использованием АТО и ATRA без цитостатических химиопрепаратов является общепринятой опцией у пациентов из группы низкого риска. Для пациентов из группы высокого риска выбор такой комбинации также возможен при добавлении небольших доз химиопрепаратов, что отражено в рекомендациях European LeukemiaNet и National Comprehensive Cancer Network.
Протокол ATRA + АТО
На протяжении более 30 лет ФГБУ «НМИЦ гематологии» Минздрава России проводит последовательные исследования, направленные на усовершенствование подходов к терапии пациентов с острыми лейкозами. Российской научно-исследовательской группой по лечению острых лейкозов также была разработана программа лечения ОПЛ, предполагающая применение АТО и ATRA. В ее основу легли результаты ранее проведенных исследований, а также собственный опыт применения этих препаратов. В настоящее время только в ФГБУ «НМИЦ гематологии» Минздрава России с 2016 года данный вариант лечения был успешно применен у более чем 200 пациентов с ОПЛ, в том числе при лечении рецидивов заболевания после ранее проведенной химиотерапии.
Наш опыт лечения пациентов с ОПЛ свидетельствует о том, что терапия с использованием ATO так же эффективна, как и химиотерапия, но значительно менее токсична, что позволяет полностью вылечить от этого заболевания всех пациентов, которым удалось выполнить программу лечения (за счет тяжести состояния в дебюте болезни некоторых больных не удается спасти).
Нехимиотерапевтический подход к лечению пациентов с ОПЛ позволил уменьшить частоту развития инфекций и зависимость от переливания компонентов донорской крови.
А токсические осложнения, связанные с ATO (нарушение функции печени и проводимости сердца), удавалось компенсировать симптоматической терапией, снижением дозы или временной отменой препарата. В настоящее время мы с радостью отмечаем, что внедрение этого подхода к лечению ОПЛ происходит и во множестве регионов России. ОПЛ – это интереснейший представитель гематологических опухолевых заболеваний, сильно выделяющийся среди своих «собратьев» благодаря особым клиническим проявлениям, биологическим тонкостям и существованию полностью нехимиотерапевтического лечения.
- Использование ATRA как производного витамина А, простого и давно знакомого вещества, оказалось весьма эффективным в борьбе с одним из самых агрессивно протекающих лейкозов.
- Использование ATO в лечении ОПЛ как ничто другое подтверждает высказывание Парацельса о том, что любой яд может быть лекарством в зависимости от дозы.



