Метод индуцированной мембраны – современный способ лечения у пациентов с остеомиелитом первой плюсневой кости при диабетической стопе
Цель данного клинического случая – предложить методику Masquelet в качестве одного из методов лечения остеомиелита плюсневой кости, как осложнения диабетической стопы. Результаты такого лечения могут положительно повлиять на прогноз и качество жизни пациентов
У людей с сахарным диабетом возникают осложнения, характеризующиеся нейропатией, лежащей в их основе. Нейропатия и ишемия приводят к нарушению целостности кожных покровов, воспалению и инфекции и могут стать причиной остеомиелита. Это частое осложнение диабета увеличивает число ампутаций сегментов конечности.
Замкнутый круг между нестабильностью костной ткани, продолжающимся ухудшением состояния мягких тканей и остеолизом создает благоприятную для бактерий среду и препятствует излечению от инфекции.
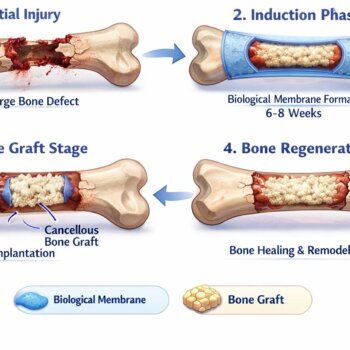
Метод Masquelet — это хирургический «инструмент», используемый при лечении костных дефектов длинных трубчатых костей. Этот метод был разработан в 1986 году Аlain C. Masquelet и его командой в больнице Авиценны во Франции. Они разработали методику реконструкции костных дефектов. Этот метод хорошо известен и хорошо изучен, используется для лечения обширной потери костной массы вследствие тяжелых травм, опухолей и инфекций. Метод включает в себя два этапа.
Метод Masquelet, также известный как метод индуцированной мембраны, представляет собой двухэтапную процедуру лечения костных дефектов. На первом этапе костные дефекты заполняются цементом из полиметилметакрилата (ПММА). Цемент из ПММА используется в качестве прокладки для устранения «мёртвых зон», системы местной доставки антибиотиков и биореакторной камеры для стимуляции остеогенеза. На втором этапе проводится остеосинтез с использованием аутотрансплантата.
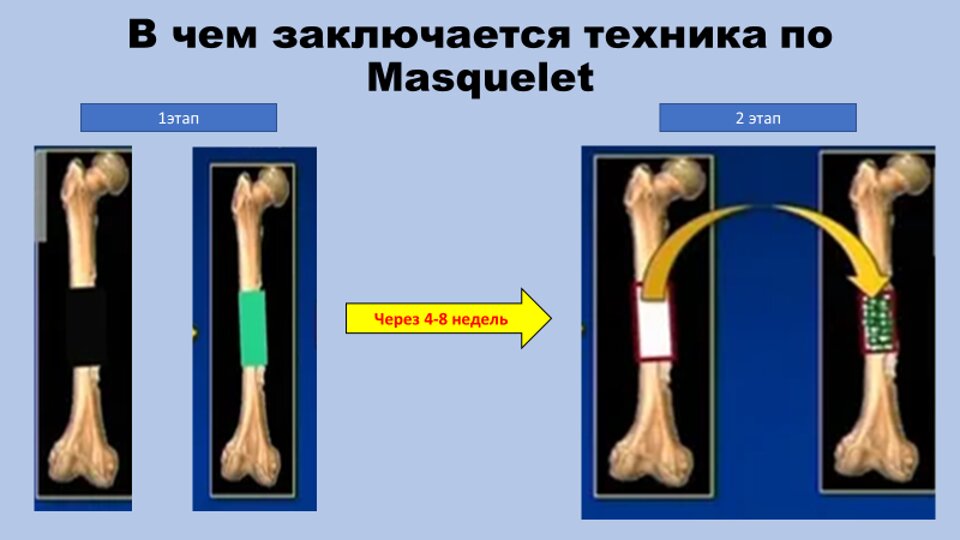
Первый этап — это тщательная хирургическая обработка с последующей установкой имплантата-спейсера из ПММА, который закрывает образовавшуюся пустоту, сохраняя нервно-сосудистые структуры, здоровые кости и мягкие ткани. Временная фиксация спейсера может быть внутренней или внешней.
Через 4-8 недель проводится второй этап — удаление цементной прокладки, повторная санация с сохранением мембраны и установка аутологичного костного трансплантата с надлежащей фиксацией кости.
Секрет успеха метода Masquelet заключается в радикальной хирургической обработке раны.
Золотой стандарт радикальной хирургической обработки раны до сих пор вызывает споры из-за того, что иногда инфекция протекает без клинических признаков и с отрицательными результатами посева на патоген. Несмотря на то, что для диагностики инфицированного несращения кости уже применяется современная технология визуализации ПЭТ-КТ, её использование ограничено из-за неудобств, связанных с обследованием.
Выявление серологических показателей инфекционного процесса, таких как интерлейкин-6 (ИЛ-6), С-реактивный белок (СРБ), количество лейкоцитов (КЛ) считается одним из диагностических тестов с высокой чувствительностью к радикальной хирургической обработке. ИЛ-6 — это новый потенциальный маркер воспаления, который вызывает всё больший интерес, в отличие от традиционных КЛ, СРБ и скорости оседания эритроцитов (СОЭ). ИЛ-6 в сыворотке крови или синовиальной жидкости показал высокую специфичность при диагностике перипротезной инфекции суставов. При лечении остеомиелита методом Masquelet интерлейкин-6 также может использоваться в качестве возможного индикатора для определения того, удалось ли устранить рецидивирующую инфекцию.
Мембрана для инкапсуляции инородного тела
Индуцированная мембрана (ИМ) — это инкапсулирующая мембрана. Она образуется в результате реакции на инородное тело, вызванной имплантацией цементной прокладки из ПММА в костный дефект. Эта реакция на инородное тело, состоящая из макрофагов и гигантских клеток инородного тела, является завершающей стадией воспалительной реакции и реакции заживления ран после имплантации любого медицинского устройства или биоматериала.
ИМ представляет собой васкуляризированную коллагеновую матрицу, в которой содержатся иммунные клетки (макрофаги, лимфоциты), а также остеокласты, участвующие в ремоделировании костной ткани, и клетки-предшественники остеобластов (мезенхимальные стволовые клетки).
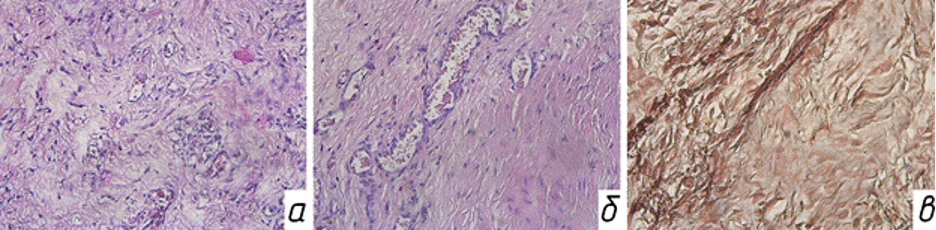
а. Фрагмент мембраны, состоящий из нежноволокнистой фиброзной ткани с множеством капилляров;
б. Нежноволокнистая фиброзная ткань с признаками отека и полнокровия сосудов;
в. Окраска трихром по Массону, показывающая нежноволокнистые соединительнотканные волокна.
С биологической точки зрения имплантационная мембрана — это камера для регенерации тканей, которая способствует интеграции костного трансплантата и формированию костной ткани тремя способами. Во-первых, мембрана действует как физический барьер между трансплантатом и окружающими его мягкими тканями, предотвращая инвазию макрофагов и последующую резорбцию трансплантата. Во-вторых, мембрана улучшает процессы ангиогенеза и остеогенеза, выделяя ключевые факторы роста, в том числе фактор роста эндотелия сосудов (VEGF), трансформирующий фактор роста-β1 (TGF-β1) и костный морфогенетический белок-2 (BMP-2).
Вкратце, VEGF-A стимулирует образование сосудистых бугорков на внутренней поверхности мембраны, которые проникают в щели костного трансплантата и обеспечивают его эффективную реваскуляризацию. BMP-2 и TGF-β1 стимулируют формирование костной ткани, способствуя остеогенной дифференцировке стволовых клеток костного мозга.
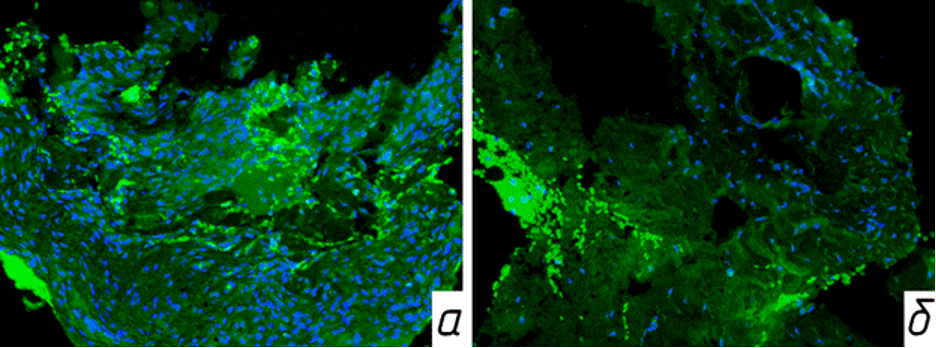
а — Иммуногистохимическое окрашивание с использованием антитела к Ki67. Активность Ki-67 в индуцированной мембране;
б — Иммуногистохимическое окрашивание с использованием антитела к CD31. Активность неоангиогенеза в индуцированной мембране.
Предварительные условия для использования
Для предотвращения неудачного применения ИМ необходимы три условия:
- предварительное устранение инфекции;
- надлежащее закрытие мягких тканей на первом этапе;
- стабильная фиксация кости на втором этапе.
Радикальное искоренение инфекции
Инфекция является наиболее частой причиной несостоятельности имплантата с мембраной. Поскольку костные трансплантаты не имеют собственной васкуляризации, на них напрямую влияет наличие микроорганизмов в мембране, что приводит к последующей резорбции трансплантата или позднему септическому рецидиву. Кроме того, инфекция изменяет остеогенные свойства имплантата с мембраной, снижая локальную экспрессию факторов роста, уменьшая количество остеобластов и стволовых клеток и повышая уровень факторов резорбции костной ткани и провоспалительных цитокинов. Таким образом, ИМ следует применять только после того, как инфекция будет окончательно устранена или, по крайней мере, взята под контроль.
Адекватное закрытие раны на первом этапе
Имплантация цементной прокладки требует не только отсутствия инфекции, но и стабильного покрытия мягкими тканями. Любой вторичный некроз кожи или расхождение краёв раны неизбежно приводит к загрязнению цементной прокладки с последующим инфицированием — неудачей имплантации цементной прокладки. Таким образом, лечение с использованием метода Masquelet часто включает реконструкцию мягких тканей с помощью лоскута на первом этапе. Выбор между микрососудистыми свободными лоскутами, лоскутами на питающей ножке (местными или отдалёнными) или свободными кожными трансплантатами зависит от контекста лечения, хирургических ресурсов и сопутствующих заболеваний.
Стабильная фиксация костных структур на втором этапе
Отсутствие механической стабильности при окончательной фиксации кости на этапе 2 является второй причиной отказа от ИМ. Недостаточная стабильность влияет на реваскуляризацию трансплантата (из-за разрыва сосудистых зачатков внутренней оболочки), что приводит к асептическому несращению и последующему отторжению. Выбор имплантата зависит от локализации дефекта, сопутствующей инфекции и предпочтений хирурга.
Длительно незаживающие раны (язвы) при синдроме диабетической стопы (СДС) являются частой причиной осложнений и ампутаций у пациентов с сахарным диабетом.
Они развиваются из-за нейропатии, внешних травм, таких как воздействие повторяющихся периодов стресса, вызванных ходьбой. И усугубляются из-за ишемии, инфекции и отека, которые играют определенную роль в развитии труднозаживающих язв. Остеомиелит часто является причиной вялотекущего развития нейропатических язв у пациентов с сахарным диабетом. У этой группы пациентов наблюдается большая склонность к инфекциям мягких тканей и костей по сравнению с теми, у кого нет диабета.
Инфицированные язвы, являющиеся наиболее частым осложнением диабетической стопы, значительно повышают рис малых и больших ампутаций. Остеомиелит встречается до 60% случаев, и его лечение является сложной задачей, вызывающей споры в зависимости от различных клинических проявлений. Стандартным методом лечения является резекция инфицированной кости, которая может привести к функциональным осложнениям и рецидивирующим язвам, что осложняет прогноз у таких пациентов.
Цель данного наблюдения — предложить методику Masquelet в качестве одного из методов лечения остеомиелита плюсневой кости как осложнения синдрома диабетической стопы. Результаты этого наблюдения могут положительно повлиять на прогноз и качество жизни этих пациентов, особенно в плане предотвращения ампутации.
Описание клинического случая
59-летний пациент поступил в отделение гнойной хирургии с жалобами на боли в левой стопе. При осмотре и пальпации был обнаружен отек, связанный с воспалительными изменениями на медиальной и дистальной областях подошвенной поверхности стопы. Проведено комплексное обследование, включая рентгенологическое и КТ стопы. Выявлена деструкция головки и диафиза первой плюсневой кости, а также и проксимальной головки основной фаланги. Результаты соответствующих лабораторных исследований показали, что уровень гликированного гемоглобина (HbA1c) составил 8,2.
В анамнезе была обнаружена медиальная подошвенная язва, которую неоднократно лечили в разных учреждениях, но без благоприятного клинического результата. На основании анамнеза и результатов параклинических исследований было принято решение о проведении хирургического вмешательства — радикальной обработки гнойно-некротического очага, включая остеотомию первой плюсневой кости от середины до головки и основной фаланги.
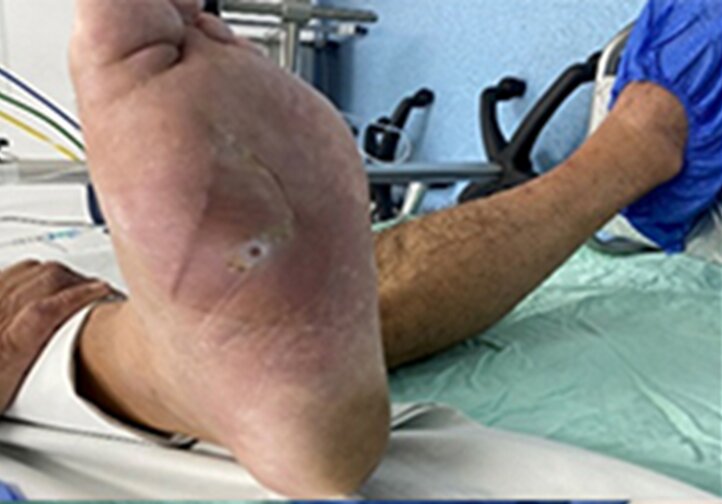
В связи с текущим состоянием пациента было принято решение применить технику Masquelet. Этот метод был выбран, чтобы пациент мог рассчитывать на благоприятный исход и избежать ампутации.
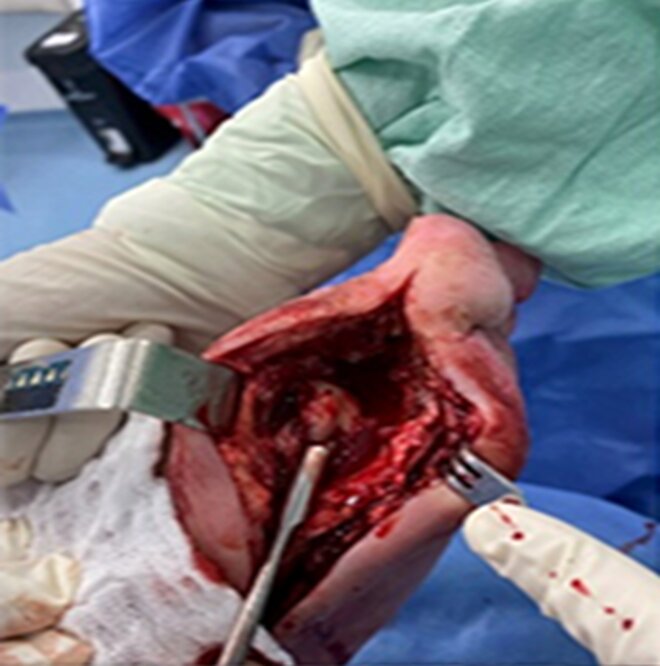
Хирургическая обработка — первый этап: удалили радикально нежизнеспособные костные фрагменты, секвестры, некротизированные и измененные мягкие ткани.
Затем подготовили спейсер. Был использован костный цемент из двух компонентов: 40 г полимерного порошка, состоящего в основном из ПММА, и 20 миллилитров жидкого мономера, состоящего в основном из метилметакрилата (ММА).
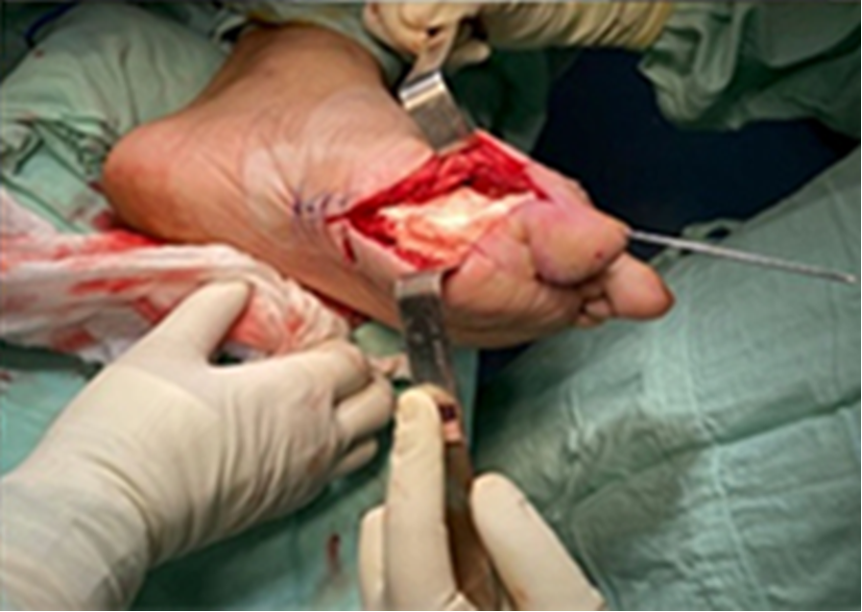
В состав цементной прокладки были включены четыре грамма нескольких термостабильных порошкообразных антибиотиков (клиндамицин, ванкомицин, меропенем и цефтазидим), отобранных на основании результата посева и антибиотикограммы.
При хроническом остеомиелите с отрицательным результатом посева включаем ванкомицин — антибиотик, широко используемый при данной технике. Он выбран благодаря своим эффективным антимикробным свойствам в отношении грамположительных бактерий, включая метициллинрезистентный S. Aureus.
С другой стороны, ванкомицин обладает высокой способностью к постоянному высвобождению из костного цемента, что обеспечивает локальную концентрацию антибиотика в очаге инфекции, помогая предотвратить рост бактерий.
Через 6 недель мы выполнили второй этап комплексного хирургического лечения.
Полиметилметакрилатную цементную прокладку удалили, сохранив мембрану в виде рукава. При осмотре искусственная мембрана имела следующие характеристики: толщина 1-3 мм; внутренняя поверхность не прилегала к прокладке, имела вид эпителия и бледно-красноватый цвет, а внешняя поверхность была прикреплена к тканям верхней плоскости.
Избегали использования инструментов, способствующих некрозу тканей, таких как термокаутер. Предварительно подготовили губчатый аутотрансплантат из гребня подвздошной кости.
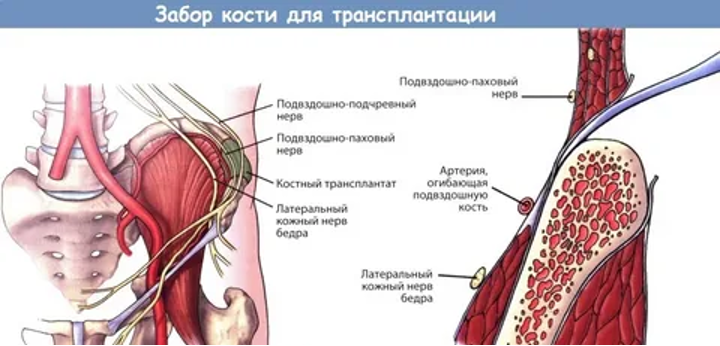
Аутологичный трансплантат гребня подвздошной кости считается золотым стандартом в качестве источника костного трансплантата в хирургии по методике Masquelet из-за различных факторов. Основным из них является относительно высокая концентрация мезенхимальных клеток (МСК), которые могут дифференцироваться в другие типы клеточных тканей, включая остеобласты, а также большое количество факторов роста, таких как TGF-B (трансформирующий фактор роста бета) и PDGF (тромбоцитарный фактор). Они играют важную роль в развитии костной ткани и пролиферации костных клеток. Костные трансплантаты фиксировали интрамедуллярно спицей Киршнера. Рану удалось закрыть местными тканями, предварительно дренировав с использованием активной аспирации.
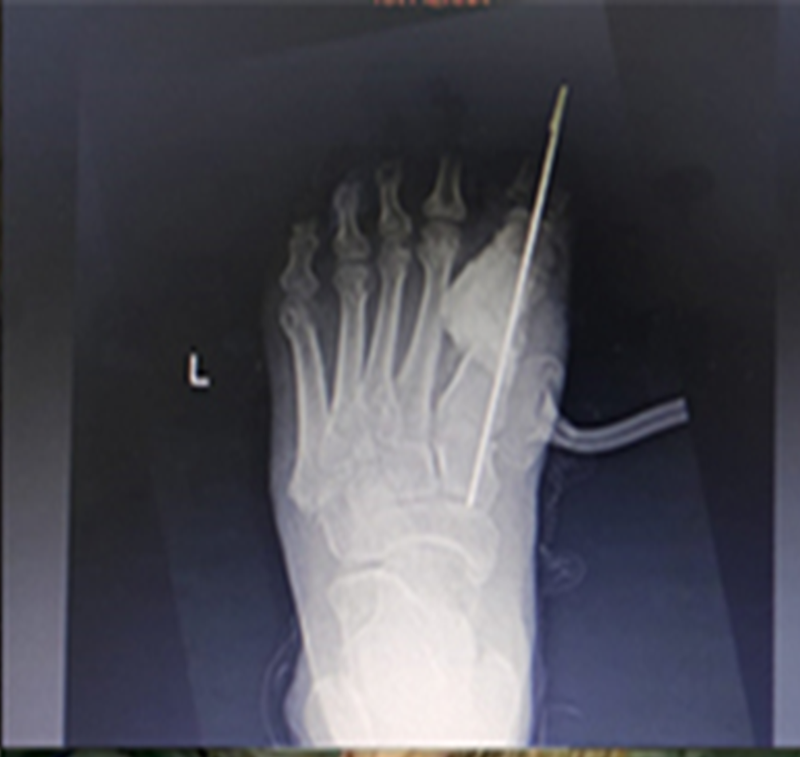
Пациенту проводили регулярные рентгенологические обследования, фиксируя время, в течение которого наблюдалась консолидация, и время, в течение которого была разрешена полная нагрузка.
Через 4 недели результаты рентгенологического исследования показали, что трансплантат без признаков лизиса и отторжения. Пациенту разрешили ходить с опорой, используя ортопедическую обувь.
Через 7 месяцев от начала лечения металлический фиксатор удален.
В настоящее время пациент ходит самостоятельно. При контрольном осмотре, лабораторном контроле, КТ и рентгенологическом исследовании область операции без каких-либо воспалительных изменений, выраженные признаки консолидации трансплантата.
Обсуждение
В связи с результатами, полученными у этого пациента, и убежденностью в том, что этот тип процедуры может принести пользу многим пациентам с такими осложнениями, как язва диабетической стопы и остеомиелит костей стопы, мы считаем: необходимы дополнительные исследования с большей методологической обоснованностью, чтобы получить больше знаний о применимости этого метода.
Выводы
Техника Masquelet — это метод, который мы должны внедрять у пациентов с сахарным диабетом. Он может улучшить качество их жизни, эффективно устраняя осложнения, связанные с остеомиелитом, и помогает сохранить функциональность.
Чтобы применить этот хирургический метод у пациентов с диабетической стопой и остеомиелитом, у них должна быть кожа без некроза. Поэтому необходимо обеспечить надлежащие условия для полного закрытия поврежденной части стопы.
Чтобы обеспечить формирование прочной костной мозоли, необходима надежная фиксация. Ортопеды знают, что для консолидации любого перелома требуется подвижность в 0,05 микрона. Если это значение превышено, перелом может перерасти в псевдоартроз.
Пациентам с диабетической стопой важно тщательно контролировать основное заболевание. Необходимо регулярно проверять общее количество белков, альбуминов и глобулинов в организме, а также уровень витаминов B12 и D3. Эти анализы должны проводиться наряду с другими параклиническими исследованиями.
Несмотря на отсутствие доказательств и сообщений об опыте широкого применения техники Masquelet при реконструкции костных дефектов стопы, в данном случае было продемонстрировано, что использование этой альтернативной хирургии дает обнадеживающие результаты.


